Serialisierung und Verifizierung
Das bedeutet Serialisierung und Verifizierung von Arzneimitteln
Eine Arzneimittelpackung wird mit einer randomisierten (zufällig gewählten) einmaligen Seriennummer ausgestattet (serialisiert), die gemeinsam mit Chargennummer und Ablaufdatum in einen zweidimensionalen Barcode verschlüsselt wird. Damit wird diese Arzneimittelpackung innerhalb Europas eindeutig identifizierbar.
Bevor ein Patient in einer Apotheke, im Krankenhaus oder beim hausapothekenführenden Arzt ein Arzneimittel bekommt, wird die Seriennummer des Medikaments überprüft (verifiziert), aus einem Datenbanksystem ausgelesen und deaktiviert. Dadurch wird die Echtheit des Medikaments sichergestellt. Sollten Unstimmigkeiten bei der Überprüfung auftreten, darf das Medikament nicht mehr abgegeben werden.

Umsetzung einer EU-Richtlinie
Seit 09.02.2019 gelten EU-weit strenge Vorgaben: Rezeptpflichtige Arzneimittel müssen mit Sicherheitsmerkmalen versehen sein. Diese stellen sicher, dass gefälschte Arzneimittel nicht in die legale Lieferkette eindringen. Grundlage dafür sind die EU Richtlinie 2011/62 des Rates und des EU Parlaments und die Delegierte Verordnung der EU Kommission 2016/161. Die Sicherheitsmerkmale umfassen das individuelle Erkennungsmerkmal und eine Vorrichtung gegen Manipulation.
Zur Erfassung der individuellen Erkennungsmerkmale wurde in jedem EU- und EWR-Staat sowie der Schweiz ein nationaler Datenspeicher eingerichtet. Das in Österreich implementierte Datenspeicher- und -abrufsystem ist, um die Überprüfung der einzelnen Arzneimittelpackungen auch innerhalb Europas zu gewährleisten, an ein europäisches System angebunden. Dieses wird von der European Medicines Verification Organisation EMVO betrieben.
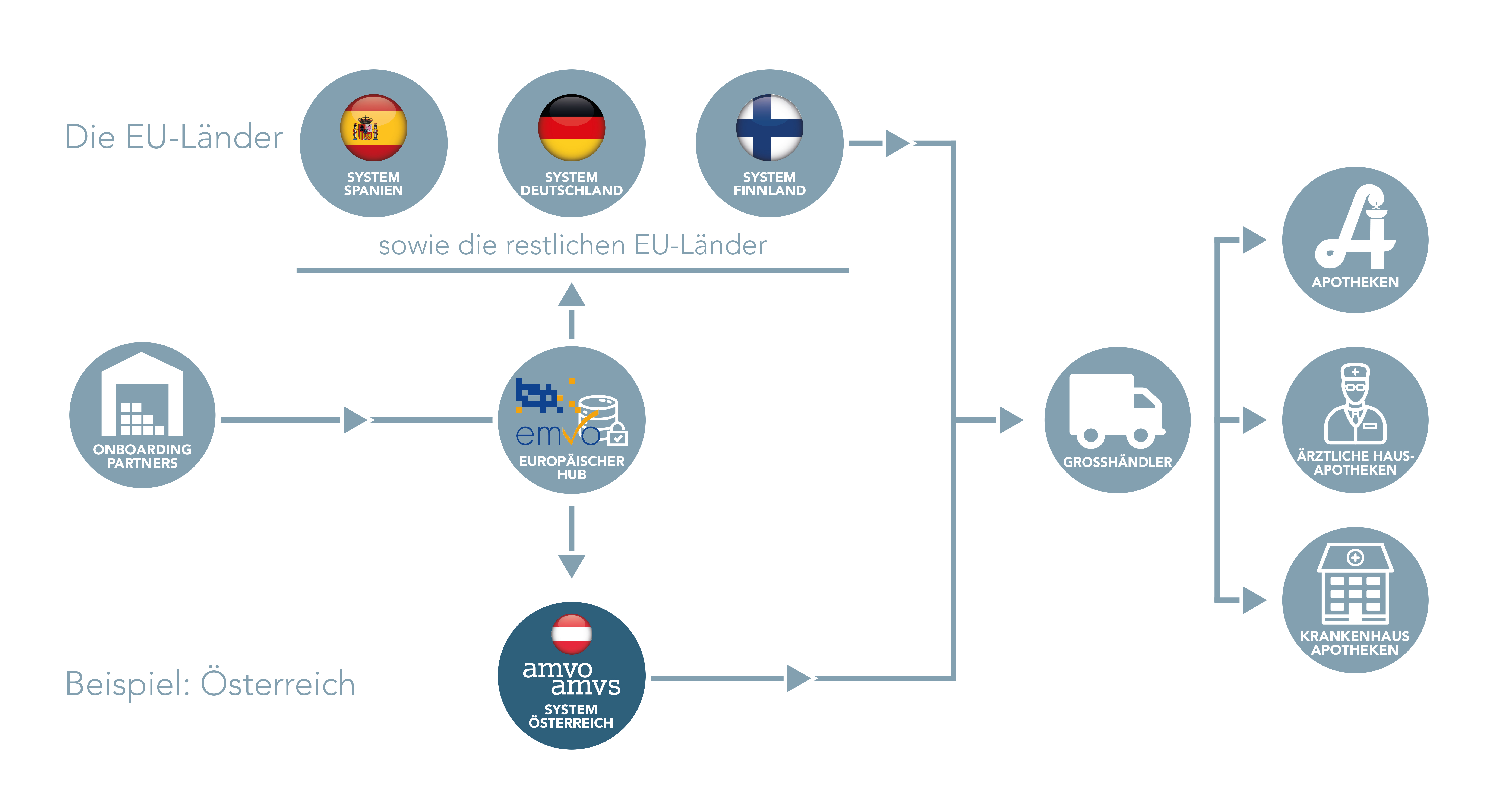
Gemäß Richtlinie und Verordnung sind alle an der pharmazeutischen Lieferkette Beteiligten selbst dafür verantwortlich, das Datenspeicher- und -abrufsystem gemeinsam zu betreiben. Die Kosten dafür sind von der pharmazeutischen Industrie zu tragen. Für die nationale Umsetzung der Fälschungsrichtlinie ist die AMVO (Austrian Medicines Verification Organisation) zuständig. In diesem Verein haben sich die Pharmig - Verband der pharmazeutischen Industrie Österreichs und der Österreichische Generikaverband für die pharmazeutische Industrie, die PHAGO - Verband der österreichischen Arzneimittel-Vollgroßhändler für den Arzneimittelgroßhandel, die Österreichische Apothekerkammer für die selbstständigen Apotheker und angestellten Apotheker in öffentlichen Apotheken und Krankenhäusern sowie die Österreichische Ärztekammer für die hausapothekenführenden Ärzte zusammengeschlossen.
Die AMVS GmbH als 100% Tochter der AMVO ist die Betreibergesellschaft für das österreichische Datenspeicher- und -abrufsystem.



